PCOS
Inhaltsverzeichnis- Bedeutung
- Ätiologie und Pathogenese
- Diagnostik
- Langzeitfolgen
- Therapie
- Zusammenfassung Therapie-Stufenkonzept
- Literatur
Bedeutung
Prävalenz im fortpflanzungsfähigem Alter 8-13%.
Ätiologie und Pathogenese
- heterogener Symptomkomplex, verschiedene Theorieansätze zur Entstehung
- starke hereditäre Komponente
- Insulinresistenz als auslösender Faktor
- Insulin steigert die ovarielle Androgenproduktion in den Thekazellen. Dies führt zu einem Ungleichgewicht zwischen den Androgenvorstufen und den im Anschluss daraus entstehenden Östrogenen in den Granulosazellen.
- Zudem führt eine Hyperinsulinämie zu einem verminderten SHBG und erhöht so den Anteil des freien Testosterons und damit die Wirkung am Androgenrezeptor.
Neuere Erkenntnisse:
- hoher Anteil der hypothalamischen GnRH-Neurone exprimiert den AMH-Rezeptor 2, beim PCOS sogar noch mehr => AMH stimuliert diese GnRH-Neurone => Amplitude wie auch Frequenz der GnRH/LH Pulse steigt, LH=> Androgensekretion am Ovar wird gesteigert
- intrauterine Programmierung durch Hyperandrogenismus der Mutter und hohe AMH-Konzentration
- erhöhte maternale Androgenwerte in Schwangerschaft = erhöhtes Risiko für metabolisches Syndrom bei der Tochter
- AMH-Werte bei PCOS Frauen in Schwangerschaft im Vgl. zu gesunden Frauen erhöht

Rotterdam Kriterien
Oligo-/Anovulation
Hyperandrogenismus (klinisch oder biochemisch)
Polyzystisches Ovar im Ultraschall oder gemäss neuer Guideline von 2023 auch erhöhtes Anti-Müller Hormon (AMH)
- zwei von drei Kriterien müssen erfüllt sein für die Diagnose PCOS
- wichtig: andere Ursachen sind ausgeschlossen, PCOS ist eine Ausschlussdiagnose!
Definition irreguläre Zyklen gemäss ESHRE
- Normal im ersten Jahr post Menarche
- > 1 bis < 3 Jahre post Menarche: < 21 oder > 45 Tage
- > 3 Jahre post Menarche bis Perimenopause: < 21 oder > 35 Tage, oder < 8 Zyklen pro Jahr
- Sekundäre Amenorrhoe > 1 Jahr post Menarche: > 90 Tage
- Primäre Amenorrhoe mit 15 Jahren oder > 3 Jahre post Thelarche
Abklärung Hyperandrogenämie: siehe auch Kapitel Hyperandrogenämie
Hyperandrogenämie
- berechnetes freies/bioverfügbares T oder freier Androgenindex (FAI) erhöht
- Messung von fT oder TT sollte massenspektrometrisch/chromatographisch erfolgen, keine Speicheltests
- Androstendion und DHEAS erhöht
Hyperandrogenismus
- Hirsutismus: modifizierter Ferriman Gallwey Score (mFGS) ≥ 4 - 6
- Alopezie: Ludwig-Score
- Akne
Sonographie/AMH
- Keine Sonographie und AMH Bestimmung für die Diagnose innerhalb der ersten 8 Jahren nach Menarche
- Entweder Sonographie oder AMH zur Diagnostik
- Sonographie: >20 AFC pro Ovar und/ oder Volumen > 10ml
- Befund unilateral reicht aus
- CAVE: Kein C. luteum, Zysten oder Leitfollikel mitzählen
- AMH korreliert mit AFC
- CAVE: AMH abhängig vom Alter, BMI, Ethnizität, Anwendung KOK und kann im Zyklus schwanken (Follikelphase höher als in der Lutealphase) => in der Guideline wird daher kein Cut-off-Wert des AMH festgelegt
Work up
- Genaue Zyklusanamnese
- Klinischer Hyperandrogenismus: Hirsutismus, androgene/diffuse Alopezie, Akne
- Ultraschall: AFC, Ovarvolumen => wenn nicht eindeutig dann Abnahme AMH
- Hormonstatus am 3.-5. Zyklustag morgens
- Berechnung freier Androgenindex (FAI = [Testosteron in ng/ml x 347] \ [SHBG in nmol/L]
- PCOS Labor (Erstdiagnose bestätigt): oraler Glucosetolerzanztest oder HbA1c, Lipide (Trigylceride, LDL, HDL, Gesamt-Cholesterin), Wiederholung je nach Risikolage und Ergebnis
- BMI
- RR (jährlich zu wiederholen)
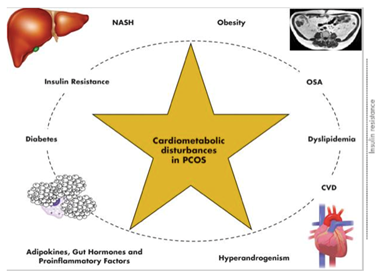
Grundsätzlich
- gute Aufklärung der Patientin über Diagnose und mögliche Langzeitfolgen
- keine Ängste generieren, jedoch Patientin motivieren einen gesunden Lebensstil zu führen!
- Kardiovaskuläres Risiko evaluieren
- Familienanamnese
Diabetes mellitus
- erhöhtes Risiko für Glukosestoffwechselstörung (T2DMx3!), gewichtsabhängig verstärkt, aber auch 75 % der schlanken Frauen mit PCOS haben eine Insulinresistenz
- oGTT ist der genaueste Test und sollte bei Frauen mit PCOS unabhängig vom BMI als Goldstandard durchgeführt werden
- HbA1c oder nüchtern Glukose nur wenn oGTT nicht durchführbar
- Test-Wiederholung alle drei Jahre wenn unauffällig
- präkonzeptionell bei jeder Frau mit PCOS: 75 g oGTT, Wiederholung alle drei Jahre wenn unauffällig
- in Schwangerschaft immer oGTT 24. SSW, in 12.-16. SSW nüchtern Blutzucker/HbA1c
Obstruktives Schlafapnoe-Syndrom
- Zusammenspiel mit PCOS unklar, ggf. spielt der Hyperandrogenismus eine Rolle in der Entstehung
- 10fach erhöhtes Risiko, steigt insbesondere mit erhöhtem BMI
- gestörter Schlaf ist ein kardiovaskulärer Risikofaktor
- Risikofaktoren erfassen mit Berliner Score möglich
Endometriumkarzinom
- Endometriumkarzinomrisiko bei anovulatorischen Zyklen erhöht
- 2-6-fach erhöht bei Oligomenorrhoe mit Zyklen >90 Tage: KOK- oder Gestagengabe empfohlen zur Zyklusregulation
- Kein Routinescreening empfohlen
Adipositas
- Bei PCOS wird eine überdurchschnittliche Gewichtszunahme beobachtet
- Appetitsteigernde/senkende Hormoneinflüsse spielen eine Rolle
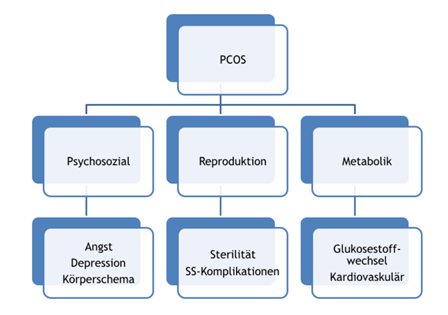
Lebensqualität
- Lebensqualität kann generell eingeschränkt sein, häufiger Angststörungen, depressive Verstimmungen, Körperschemastörungen, Essstörungen und psychosexuelle Funktionsstörungen.
Therapie
Lifestyle Interventionen
- Lebenslang gilt: Bewegung und Vermeidung Übergewicht
- Alle 6-12 Monate Gewichtsveränderung dokumentieren
- Diät, Sport und Verhaltensänderung bei Übergewicht
- Kalorienzufuhr: 1.200 bis 1.500 kcal/Tag
- Kalorienreduktion egal mit welcher Art von Diät, Studien konnten keine Überlegenheit einer Diätform zeigen, Empfehlung zur gesunden Ernährung
- Zur Prävention von Gewichtszunahme:
- 18 – 64 J: mind. 150 Min/Woche moderate Intensität oder 75 min/Woche hohe Intensität oder Kombination beider
- Muskelaufbau an zwei nicht aufeinanderfolgenden Tagen
- Mind. 30 Minuten in mindestens 10-minütigen Perioden
- Zur Gewichtsreduktion:
- Mind. 250 Min/Woche moderate Intensität oder 75-150 min/ Woche hohe Intensität oder Kombination beider
- Muskelaufbau an zwei nicht aufeinanderfolgenden Tagen
- Minimieren von sitzenden Tätigkeiten
- 5-10% Gewichtsverlust innerhalb von 6 Monaten anstreben
- Benefit durch Bewegung auch ohne Gewichtsverlust
- Täglich 10.000 Schritte anstreben
- SMART (Specific, Measurable, Achievable, Realistic and Timely)
Pharmakologische Massnahmen zur Gewichtsreduktion
- Orlistat oder GLP-1-Rezeptor-Agonisten (Liraglutid, Semaglutid) begleitend zu Lifestyle Interventionen bei Erwachsenen mit Adipositas evaluieren (Diabetologie)
- Effektive Kontrazeption bei Anwendung von GLP-1-Rezeptor Agonisten, da Sicherheitsdaten in der Schwangerschaft und bei Kinderwunsch bislang fehlen
- CAVE: gastrointestinale Nebenwirkungen, erneute Zunahme nach Absetzen der Medikation und bislang fehlen Langzeitdaten zur Sicherheit des Medikaments
Operative Massnahmen zur Gewichtsreduktion
- zu evaluieren bei BMI > 35 kg/m oder BMI 30-34.9 mit zusätzlichen Risikofaktoren und bisher frustranen alternativen Therapien.
Kombinierte orale Kontrazeptiva
- Frauen mit PCOS und Hyperandrogenismus (Hirsutismus/Alopezie) und/oder unregelmässigem Menstruationszyklus sowie Wunsch nach Antikonzeption
- Prinzipiell ist jeder kombinierte Ovulationshemmer einsetzbar, tendenziell Gestagene mit Androgenpotenzial eher meiden.
- Jede Pille mit Estrogen (E2) hat einen antiandrogenen Effekt, Effekt aber natürlich besser mit inertem oder antiantrogenem Gestagen
- Somit besser kein Levonorgestrel oder Norethisteron!
- Pillen mit Dienogest empfehlenswert
- Pille mit 35μg E2+CPA primär nicht empfohlen -> erhöhtes Risiko für thromboembolische Ereignisse
- SGGG-Checkliste immer ausfüllen vor Verschreibung, Patientinneninformation abgeben
- Therapieversuch mind. 6 Monate, das heisst Einfluss auf Hirsitusmus erst nach 6-9 Monaten zu beurteilen
- ggf. Kombination mit kosmetischer Therapie (z.B. Eflornithin (Vaniqua®), Lasertherapie)
Auflistung Antiandrogene Pillen
Metformin
- Antidiabetischer und blutzuckersenkender Wirkstoff aus der Gruppe der Biguanide
- Effekt durch erhöhte Empfindlichkeit des Muskels, Fettgewebe, Ovarien für Insulin, Hemmung der Gluconeogenese in der Leber, Senkung der Aufnahme im Darm
- Empfohlen bei einem BMI ≥ 25kg/m2 (metabolischer Benefit höher als bei niedrigerem BMI) zusätzlich zu Lifestyle-Massnahmen Gewichtsreduktion, Verbesserung der metabolischen Situation
- Datenlage zu Einsatz bei BMI < 25 und in der Adoleszenz weniger gut
- KOK zur Therapie von Androgenisierungserscheinungen und irregulärer Zyklen ist im Vgl zu Metformin überlegen. Kombinationstherapie aus KOK und Metformin bei BMI < 30 bietet wenig zusätzliche Nutzen im Vergleich zur Monotherapie (KOK oder Metformin allein).
- Zu wenig Evidenz für Empfehlung zur Zyklusregulierung durch Metformin,keine Evidenz bei isoliertem Hirsutismus
Bei Verschreibung folgendes beachten:
- NW wie gastrointestinale Symptome (Übelkeit, Erbrechen, Diarrhö, Bauchschmerzen) meist dosisabhängig und selbstlimitierend
- Low dose Start mit z.B. 500mg/d und Erhöhung 1-2 wöchentlich auf Zieldosis 1500mg; evtl. extended release Präparat (senkt Rate NW und erhöht Compliance)
- Off label use! Gute Aufklärung der Patienten
- Bei Langzeittherapie Vit.B12 Spiegel beachten
- Therapiebeendigung bei Schwangerschaft (keine KI, begrenzte Erfahrungen, keine Evidenz für Benefit)
Inositol
- Inositol ist ein Isomer der Glukose und kommt sowohl in Pflanzen als auch tierischem Gewebe vor. Beispielsweise haben Zitrusfrüchte relative hohe Konzentrationen an Myo-Inositol. Inositol kann vom Körper auch direkt synthetisiert werden wie z. B. in der Niere oder in anderen Organen
- Inositol spielt als „second messenger“ bei vielen Stoffwechselvorgängen eine zentrale Rolle
- Kann zu Verbesserung der Hyperandrogenämie und metabolischer Parameter (Lipide, HOMA) führen, Evidenzlage schlecht
- Nutzen in Bezug auf Ovulation, Reduktion Hirsutismus, Gewicht ist limitiert
- Metformin ist dem Inositol überlegen
Zusammenfassung Therapie-Stufenkonzept
- Änderung des Lebensstils: Sport, Diät etc.
- Systemische Behandlung:
- KOK
- Antiandrogene KOK
- wenn nach 6-9 Monate keine Besserung, dann eine Kombination von antiandrogener Pille mit zunächst niedrig dosiertem CPA (z.B. Androcur)
- Bei Adipositas/metabolischen Faktoren Metformin evaluieren
- Lokale Behandlung (Laser + Eflornithin z.B. Vaniqua®)
Literatur
- International evidence-based guideline for the assessment and management of polycystic ovary syndrome (PCOS), ESHRE 2023
Autor: L. Gabriel
Autorisiert: K. Schiessl
KSW Version: 3.0, 12/2024
